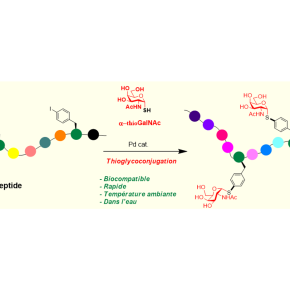
Une voie d’accès inédite à des peptides stables en milieu biologique
C'est une avancée notable dans la chimie des sucres. Les chimistes du laboratoire de Biomolécule-Conception, Isolement et Synthèse (CNRS/Université Paris-Sud) et du Centre de Biophysique Moléculaire (CNRS), ont mis au point une méthode simple et originale pour synthétiser des peptides thioglycosylés. Ces conjugués d’un peptide et d’un sucre dont l'oxygène est remplacé par un soufre sont très stables dans un milieu biologique. Ces travaux, publiés dans la revue Chemical Science, ouvrent de multiples applications en thérapie et en recherche.
Les glycopeptides et les glycoprotéines sont des conjugués composés d’un sucre lié à une chaîne d’acides aminés (peptide) ou à une protéine. Ils constituent l’architecture moléculaire de nombreuses biomolécules et ils sont largement présents dans tous les organismes vivants. Cette omniprésence les rend indispensables notamment en médecine mais la liaison du sucre au peptide/protéine peut se faire dégrader par les enzymes présentes dans le vivant. Pour suivre un glycoconjugé particulier ou pour délivrer un glycoconjugé à usage médical, il faut donc le rendre inattaquable par ces enzymes. Ce que des chimistes du laboratoire de Biomolécule-Conception, Isolement et Synthèse (CNRS/Université Paris-Sud) et du Centre de Biophysique Moléculaire (CNRS) viennent de réaliser avec une méthode plus simple qu’auparavant.